| Nom complet officiel |
Facteur inhibiteur de la leucémie humaine recombinante (rHuLIF) |
| Séquence |
 |
| Séquence d'acides aminés |
SPLPITPVNA TCAIRHPCHN NLMNQIRSQL AQLNGSANAL FILYYTAQGE PFPNNLDKLC GPNVTDFPPF HANGTEKAKL VELYRIVVYL GTSLGNITRD QKILNPSALS LHSKLNATAD ILRGLLSNVL CRLCSKYHVG HVDVTYGPDTKK SGKDVFQQAV |
| synonymes |
Facteur stimulant la différenciation, facteur D, inhibiteur de la LPL dérivé du mélanome, MLPLI |
| Numéro d'accès |
P15018 |
| Identifiant du gène |
3976 |
| Résumé |
Le facteur inhibiteur de leucémie (LIF) est un membre de la famille des interleukines 6. Cette protéine est principalement exprimée dans le trophectoderme de l'embryon en développement, son récepteur LIFR étant exprimé dans toute la masse cellulaire interne. Le LIF a la capacité d'induire une différenciation terminale dans les cellules leucémiques. Ses activités comprennent l'induction de la différenciation hématopoïétique dans les cellules leucémiques normales et myéloïdes, l'induction de la différenciation des cellules neuronales et la stimulation de la synthèse des protéines en phase aiguë dans les hépatocytes. Le LIF est utilisé dans la culture de cellules souches embryonnaires de souris, car cette élimination du LIF pousse les cellules souches vers la différenciation, mais elles conservent leur potentiel de prolifération ou leur pluripotence. Il est également utilisé dans un essai clinique de phase II, qui peut aider à l'implantation d'embryons chez les femmes qui n'ont pas réussi à devenir enceintes malgré les technologies de procréation assistée (ART). Le LIF humain mature (180 aa) partage 78 %, 82 %, 91 %, 88 % et 87 % d'identité de séquence aa avec le LIF de souris, de rat, de chien, de bovin et de porc, respectivement. |
| Identifier |
Escherichia coli. |
| Masse moléculaire |
Environ 19.7 kDa, une seule chaîne polypeptidique non glycosylée contenant 180 acides aminés. |
| Activité biologique |
Entièrement biologiquement actif par rapport à la norme. La DE50 déterminée par la prolifération dose-dépendante des cellules TF-1 humaines est inférieure à 0.1 ng/ml, correspondant à une activité spécifique > 1.0 × 107 UI/mg. |
| Aspect |
Poudre lyophilisée blanche filtrée stérile (lyophilisée). |
| Formulation |
Lyophilisé à partir d'une solution concentrée filtrée de 0.2 um dans du PBS, pH 7.4. |
| Endotoxine |
Moins de 1 UE/ug de rHuLIF tel que déterminé par la méthode LAL. |
| Reconstitution |
Nous recommandons que ce flacon soit brièvement centrifugé avant ouverture pour ramener le contenu au fond. Reconstituer dans de l'eau distillée stérile ou un tampon aqueux contenant 0.1 % de BSA à une concentration de 0.1 à 0.2 mg/mL. Les solutions mères doivent être réparties en aliquotes de travail et conservées à ≤ -20 °C. D'autres dilutions doivent être effectuées dans des solutions tamponnées appropriées. |
| Stabilité et stockage |
Utiliser un congélateur à dégivrage manuel et éviter les cycles de gel-dégel répétés.- 12 mois à compter de la date de réception, -20 à -70 °C tel que fourni.- 1 mois, 2 à 8 °C dans des conditions stériles après reconstitution.- 3 mois, -20 à -70 °C dans des conditions stériles après reconstitution. |
| Bibliographie |
|
| SDS-PAGE |
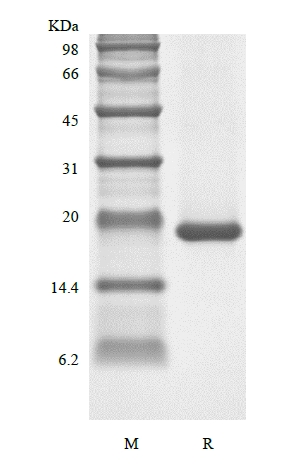 |
| Télécharger la fiche de données de sécurité (FDS) |
Cliquer pour télécharger |
| Télécharger la fiche technique (TDS) |
Cliquer pour télécharger |



