| Nom complet officiel |
Facteur de nécrose tumorale humaine recombinant-alpha/TNFSF2 GMP (rHuTNF-alpha/TNFSF2) |
| Séquence |
 |
| Séquence d'acides aminés |
MVRSSSRTPS DKPVAHVVAN PQAEGQLQWL NRRANALLAN GVELRDNQLV VPSEGLYLIY SQVLFKGQGC PSTHVLLTHT ISRIAVSYQT KVNLLSAIKS PCQRETPEGA EAKPWYEPIY LGGVFQLEKG DRLSAEINRP DYLDFAESGQ VYFGIAL |
| synonymes |
Facteur de nécrose tumorale, TNFSF2, Cachectine, Facteur inducteur de différenciation, DIF, Nécrosine, Cytotoxine |
| Numéro d'accès |
P01375 |
| Identifiant du gène |
7124 |
| Résumé |
Le facteur de nécrose tumorale alpha (TNF-alpha), également appelé cachectine, est le membre le plus connu de la famille des TNF, qui peut provoquer la mort cellulaire. Cette protéine est produite par les neutrophiles, les lymphocytes activés, les macrophages, les cellules NK, les cellules LAK, les astrocytes, les cellules endothéliales, les cellules musculaires lisses et certaines cellules transformées. Le TNF-alpha se présente sous une forme soluble sécrétée et sous une forme ancrée dans la membrane, qui sont toutes deux biologiquement actives. La forme naturelle du TNF-alpha est glycosylée, mais le TNF-alpha recombinant non glycosylé a une activité biologique comparable. La forme native biologiquement active du TNF-alpha serait un trimère. Le TNF-alpha humain et murin présente une homologie d'environ 79 % au niveau des acides aminés et une réactivité croisée entre les deux espèces. Deux types de récepteurs du TNF-alpha ont été décrits et pratiquement tous les types cellulaires étudiés montrent la présence d'un ou des deux types de récepteurs. |
| Identifier |
Escherichia coli. |
| Masse moléculaire |
Environ 17.5 kDa, une seule chaîne polypeptidique non glycosylée contenant 158 acides aminés. |
| Activité biologique |
Entièrement biologiquement actif par rapport à la norme. La DE50 déterminée par un test de cytotoxicité utilisant des cellules murines L929 est inférieure à 0.05 ng/ml, correspondant à une activité spécifique > 2.0 × 107 UI/mg en présence d'actinomycine D. |
| Aspect |
Poudre lyophilisée blanche filtrée stérile (lyophilisée). |
| Formulation |
Lyophilisé à partir d'une solution concentrée filtrée à 0.2 um dans 10 mM de PB, 10 mM de NaCl, pH 7.0. |
| Endotoxine |
Moins de 0.01 UE/ug de rHuTNF-α/TNFSF2 GMP tel que déterminé par la méthode LAL. |
| Reconstitution |
Nous recommandons que ce flacon soit brièvement centrifugé avant ouverture pour ramener le contenu au fond. Reconstituer dans de l'eau distillée stérile ou un tampon aqueux contenant 0.1 % de BSA à une concentration de 0.1 à 1.0 mg/mL. Les solutions mères doivent être réparties en aliquotes de travail et conservées à ≤ -20 °C. D'autres dilutions doivent être effectuées dans des solutions tamponnées appropriées. |
| Stabilité et stockage |
Utilisez un congélateur à dégivrage manuel et évitez les cycles de gel-dégel répétés.- Un minimum de 12 mois lorsqu'il est stocké à ≤ -20 °C tel que fourni. Se référer au COA spécifique au lot pour la date de péremption.- 1 mois, 2 à 8 °C dans des conditions stériles après reconstitution.- 3 mois, -20 à -70 °C dans des conditions stériles après reconstitution. |
| Bibliographie |
1. Davenport C, Kenny H, Ashley DT et coll. 2012. Eur J Clin Invest, 42 : 1173-9.2. Cavalcanti YV, Brelaz MC, Neves JK et al. 2012. Pulm Med, 2012 : 745483.3. Sheng WS, Hu S, Ni HT et al. 2005. J Leukoc Biol, 78 : 1233-41.4. Berthold-Losleben MandHimmerich H. 2008. Curr Neuropharmacol, 6 : 193-202. |
| SDS-PAGE |
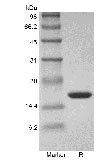 |
| Télécharger la fiche de données de sécurité (FDS) |
Cliquer pour télécharger |
| Télécharger la fiche technique (TDS) |
Cliquer pour télécharger |



